Tarihçeye bakacak olursak preinvaziv lezyonlar ilk kez 1900 yılında Cullen tarafından uterusda invaziv olmayan lezyonlara ithafen fullanılmıştır.Ardından Schaueristein (1908), Pronai (1909), ve Rubin (1910) süperfisial metaplastik epitelin yassı hücreli karsinomun erken evresi olduğunu ileri sürmüşlerdir. 1927 yılında Schiller preinvaziv neoplazi kavramını destekleyen bulgular sunmuş ve Broders 1932 yılında ilk kez karsinoma insitu (CIS) terimini kullanmıştır. 1940’larda ise Papanicolau eksfoliatif sitolojiyi gündeme getirmiş ve uterin ve servikal kanserlerin taramasında kullanılmasını önermiştir.1950’lerde de Amerikan kanser derneği servikal sitolojinin tarama amaçlı kullanılmasını desteklemiştir (1).
Preinvaziv servikal hastalık kavramı ise 1947 yılında invaziv kanser görünümüne sahip ancak epitele nınırlı değişiklikleri tanımlamak için kullanılmıştır. Reagan ve arkadaşları 1956’da CIS ile normal epitel arasındaki histolojik ve sitolojik farklılıkları gösteren anormallikleri displazi olarak adlandırmış; hafif, orta ve şiddetli olmak üzere 3 gruba ayırmıştır. 1961 yılında 1. Uluslararası Eksfoliatif Sitoloji Kongresi’nde CIS teriminin epitelin tüm kalınlığının farklılaşmamış neoplastik hücreler tarafından oluşturulan lezyonlar için kullanılmasına karar verilmiştir. Displazi ve CIS’ın sürekli bir olayın farklı basamaklarını teşkil ettiğini düşünen Richart, 1967 yılında servikal intraepitelial neoplazi (CIN I, II, III ) terimini tanımlamıştır. Sonraki çalışmalar bu lezyonların tedavi edilmemeleri halinde servikal kansere yol açabileceğini gösterdi (1).
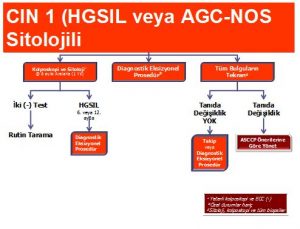
2001 Bethesda sisteminin sitolojik anormallikler için kullanılmaya başlamasi ile birlikte klinik terminolojimize serviks kanserine dönüşme potansiyeli olan lezyonları tanımlamak için, LSIL (Low (Düşük) dereceli skuamoz intraepiteliyal lezyon) ve HSIL (Yüksek dereceli skuamoz intraepiteliyal lezyon) terimleri girmiştir. Histolojik sınıflamada CIN1,düşük dereceli lezyonları CIN2,3 ise yüksek dereceli lezyonları içermektedir. Sitolojik LSIL’in histolojik CIN1’e ve sitolojik HSIL’in histolojik CIN 2,3’e eşit olmadığı da daima akılda tutulmalıdır (1).
Bu derlemede servikal preinvaziv lezyonların tanımı, dünyada ve ülkemizde görülme sıklığı ve Amerikan servikal patoloji ve kolposkopi derneği tarafından önerilen yönetim algoritması özetlenecektir.
Servikal Intraepitelyal Neoplazi Tanımı ( CIN 1,2,3) Nedir , Neden Oluşur , Histolojisi ve Sınıflaması:
Anormal servikal lezyonlar ; epitelin alt 1/3’ünde sınırlı ise Servikal Intraepiteliyal Neoplazi I(CIN I) , alt 2/3’ünde ise CIN II, epitelin tamamına yakını tutulmuş ise CIN III, tamamını içeriyorsa Karsinoma İn Situ (CIS) olarak adlandırılır. Bütün lezyonlarda bazal membran sağlamdır. Fakat CIN’lerde invazyon potansiyeli her aşamada vardır.
İnvaziv servikal kanserler genellikle uzun bir preinvaziv hastalık evresini izlerler. Mikroskopik olarak, invaziv karsinomlara ilerlemeden önce hücresel atipiden, değişen derecelerde servikal intraepitelyal neoplazilere (CIN) ilerleyen prekürsor lezyonlar spektrumu ile karakterizedir. Epidemiyolojik çalışmalar, CIN ve servikal kanser gelişimine katılan bir dizi risk faktörü belirlemiştir fakat günümüzde en önemlisi HPV olarak kabul edilmektedir (11).
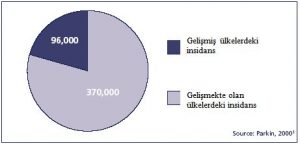
10-15 yıllık uzun bir preinvazif döneme sahip olması, sitolojik tarama yöntemlerinin mevcudiyeti ve preinvazif lezyonların etkin şekilde tedavi edilebilmesi nedeniyle invazif serviks kanserinin önlenebilir bir kanser olduğu düşünülür. Nitekim serviks kanseri tüm kanserler arasında koruyucu yaklaşımlarda en fazla başarı elde edilendir. Buna rağmen ABD’de 2003 yılında 12.200 yeni invazif serviks kanseri vakası ve buna bağlı 4100 ölüm olduğu saptanmıştır. Serviks kanseri endometrium ve over kanseri sonrası 3. en sık jinekolojik kanserdir ve over ve endometrium kanserinden sonra 3. en sık jinekolojik kansere bağlı ölüm nedenidir (2). Gelişmekte olan ülkelerde ise halen en sık jinekolojik kanser serviks kanseridir ve bu ülkelerde tanı anında hastaların büyük kısmında hastalık ileri evrededir, bu ise hastalığın mortal seyretmesine neden olmakladır (Şekil 1) (3).
Serviks kanserinin ortalama görülme yaşı yaklaşık 53’tür (4). Hastalık bimodal bir yaş dağılımı gösterir, 35-39 ve 60-64 yaşlarında en yüksek insidanslara rastlanır. (1).
HPV nin Yolaçtığı Serviks kanseri gelişimi için çeşitli risk faktörleri vardır, bunlar (4):
⦁ Erken yaşta (16 yaştan önce) ilk koitus
⦁ Multipl cinsel partner
⦁ Başta Human Papilloma Virus (HPV) enfeksiyonu olmak üzere cinsel yolla bulaşan hastalıklar
⦁ Sigara içimi (aktif veya pasif)
⦁ Irk
⦁ Yüksek parite
⦁ Düşük sosyoekonomik düzey
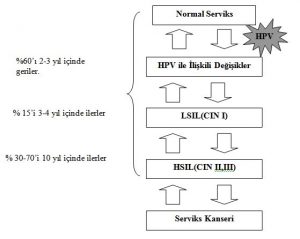
Servikal kanserin gelişimi uzun sürede olur, adolesan çağda lezyonlar genellikle düşük gradelidir ve bu lezyonların çoğu spontan olarak regrese olur, az bir kısmı ise servikal intraepitelyal neoplazilere (CIN’lere) dönüşür. CIN 1,2 ve 3’ün median görülme yaşları sırasıyla 25,29 ve 34’tür (5). CIN 1’in en az 2/3’ü, CIN 2’nin yarısı ve CIN 3’ün 1/3’ü regrese olur, en sonunda lezyonların küçük bir oranı invazif kansere ilerler (3).
HPV, ASCUS, LSIL, HSIL , ASC-H Nedir ? HPV, ASCUS, LSIL, HSIL , ASC-H Nasıl Tanı Konur ? HPV, ASCUS, LSIL, HSIL , ASC-H Nasıl Tedavi Edilir ? ASCUS smear sonucu hakkında sorular :
Servikal displazi ve karsinogenezde başlatıcı etken Human Papilloma Virus (HPV) enfeksiyonudur. Genital HPV enfeksiyonu günümüzde dünya çapında en sık rastlanan cinsel yolla bulaşan hastalıktır (6). Cinsel açıdan aktif bireylerde yaşam boyu HPV enfeksiyonu riskinin %80-85 olduğu tahmin edilmektedir (7). Serviks tümörlerinin %99’undan fazlasında HPV-DNA saptanır (8).
Serviks özellikle skuamoz metaplazinin en aktif olduğu adolesan dönemde bu enfeksiyona açıktır. Nitekim HPV prevalansının en yüksek olduğu yaş grubu 20-24, daha sonra ise 15-19’dur. Çoğu kadın, özellikle de genç yaştakiler etkin bir immün yanıt vererek ortalama 1-2 yıl içinde enfeksiyonu temizler veya viral yükü saptanamayacak düzeylere indirir (9). Böylece 30 yaştan sonra prevalans hızla azalır, bunda en önemli etken enfeksiyona yatkın olan transformasyon zonunun yaşla regrese olmasıdır. Ama sigara içenlerde ve immün yetmezliği olanlarda bu enfeksiyon epitelde premalign ve preinvazif lezyonlara ilerleyebilir (10). Buna göre serviks kanseri, hassas kişilerde yüksek riskli HPV tiplerinin seksüel yolla bulaşan enfeksiyonuna yanıt olarak meydana gelir.
Gençlerde HPV enfeksiyonu çok sık olduğu ve yaşla spontan regresyon ihtimali fazla olduğu için HPV testinin 30 yaşın üzerindeki kadınlarda uygulanması halinde yüksek gradeli lezyonların tespitinde spesifitenin artacağı saptanmıştır (11).
HPV’nin 100’den fazla tipi tanımlanmıştır. Yüksek riskli tipler intraepitelyal neoplazilerle ilişkilidir ve kansere ilerleme ihtimali bu tipler varlığında daha fazladır. Bu tipler arasında en sık görülen ve en karsinojenik olanlar tip 16 ve 18’dir. Düşük riskli tipler ise daha çok genital kondilomlardan sorumludur ve bunlardan en sık görülenler tip 6 ve 11’dir (11). İlk HPV enfeksiyonu ile invazif kanser arasındaki süre ortalama 15 yıldır (Şekil 3) (12) .
Sitolojik tarama sayesinde preinvazif evrede tanı koyulan hastalarda invazif hastalık oluşmasını engelleyecek etkili tedavi modaliteleri de mevcuttur (18). Yeni serviks kanseri tanılarının %25-30’undan örnekleme veya yorumlama hataları, %50-60’ından ise taramanın hiç yapılmaması veya suboptimal yapılması sorumlu tutulmaktadır (19). Serviks kanseri tanısı konan hastaların yarısı hiç smear testi yaptırmamış, %10’u ise son 5 yıl içinde taranmamıştır (Tablo 1,2) (20).
Pap smearın bu başarısına rağmen yapılan bir meta-analizde servikal kanseri saptama açısından sensitivitesinin %51, spesifitesinin %98 olduğu bulunmuştur (20). Bu nedenle Pap testi ile ilgili en önemli limitasyon yüksek yalancı-negatif oranlardır ve bu oran %5-10 olarak bildirilmiştir. Bu verilere göre her 10-20 pozitif vakanın 1 tanesi rutin konvansiyonel Pap smear taraması ile atlanmaktadır. Yalancı-negatif sonuçların 2/3’ünün örnekleme hatalarından, 1/3’ünün ise yorumlama hatalarından kaynaklandığı tahmin edilmektedir (22). Bunu telafi etmek için testin belli aralarla tekrarlanması önerilir, bu sayede sensitivite artırılarak yalancı-negatif sonuçlardan kaynaklanan medikolegal sorunların önüne geçilmesi amaçlanır.
Anormal Servikal Sitoloji Sonucu Olan Hastalarda Yönetim , (ASCUS tedavisi, LSIL tedavisi, HSIL Tedavisi, AGC tedavisi ) ASCUS Neden olur ?
Önemi belirlenememiş ATİPİK hücreler anlamına gelmekte olup (ASCUS) dikkatlice değerlendirilmelidir.
ABD’de yılda yaklaşık 50 milyon Pap test yapılmakta ve bunların yaklaşık 3.5 milyonunda (%7’sinde) ileri değerlendirme veya izlem gerektiren bir sitolojik anormallik saptanmaktadır (37, 38). Eylül 2001’de American Society for Colposcopy and Cervical Pathology (ASCCP) sitolojik anormallik saptanan hastalardaki uygun yönetimle ilgili bir konsensus konferansı düzenlemiştir. Burada sitolojik klasifikasyon için 2001 Bethesda Sistemi kullanılmıştır. Ardından bu konsensus guideline’ı 2006 ‘da tekrar revize edilmiştir. Bu konsensus toplantısına göre sitolojik anormallik saptanan hastalarda uygun yönetim aşağıda anlatıldığı şekilde olmalıdır (21)
Kolposkopi Nedir ? Kolposkopi Nasıl Yapılır ? Kolposkopi Ankara
Kolposkopi, anormal sitoloji sonucu olan hastalarda rahim ağzı kanseri öncülü olabilecek lezyonların ileri incelenmesi için kullanılan bir büyüteçdir. Kolposkopi rahim ağzının mikroskop ya da dürbüne benzeyen özel bir büyüteç yardımı ile incelenmesidir. Kolposkop adı verilen bu alet, normal jinekolojik muayene sırasında çıplak gözle izlenen rahim ağzının daha büyük, net ve detaylı şekilde gözlenmesine olanak tanır. İşlem esnasında rahim ağzına bazı boya ve maddeler uygulanarak şüpheli alanların daha belirgin hale gelmesi ve biopsi alınması gereken bu alanların saptanması sağlanır.
Kimlere kolposkopi Yapılır ?
Kolposkopi ve biopsi yapılmasını gerektiren durumlar şunlardır:
⦁ PAP smear sonucu rahim ağzını oluşturan hücrelerde şiddetli ya da orta şiddette kansere dönüşme potansiyeli taşıyan değişim (displazi) saptanan kadınlar. (Smear sonucu ASCUS, , ASC-H,LSIL,HSIL, CIN II-III )
⦁ Muayenede serviksin anormal görünüşlü olması
⦁ Sitoloji histoloji uyumsuzluğu olması
⦁ ilişki sonrası kanama olması
Atipik skuamoz hücreler (ASC) Nedir ? Atipik skuamoz hücreler (ASC) nasıl tedavi edilir ?
HPV, ASCUS, LSIL, HSIL , ASC-H Nedir ? HPV, ASCUS, LSIL, HSIL , ASC-H Nasıl Tanı Konur ? HPV, ASCUS, LSIL, HSIL , ASC-H Nasıl Tedavi Edilir ?
Tüm smearların %4,4’ünde atipik skuamoz hücreler saptanır. Bu hücreler de Bethesda değerlendirme sistemine göre ASC-US (ASC of undetermined significance) ve ASC-H (ASC-cannot exclude high grade lesion) şeklinde 2’ye ayrılır. Smear sonucunda ASC rapor edilen hastanın yönetiminde dikkate alınması gereken bir çok faktör vardır. Bu tür bir sitoloji sonucu olan hastalarda biyopsi konfirmasyonlu CIN 2,3 oranı %5-17’dir. CIN 2,3 oranı ASC-H tanısı alan hastalarda ise %24-94’tür. ASC-H rapor edilen bir hastanın HSIL’e eşdeğer olduğu unutulmamalıdır. Atipik skuamoz hücreler varlığında invazif kanser riski %0,1-0,2’dir. Biyopsi ile konfirme edilmiş CIN yoksa bu tür hastalarda diagnostik eksizyonel prosedürlerin rutin şekilde uygulanması önerilmez.
ALTS çalışmasından ve diğer çalışmalardan elde edilen veriler ASC-US rapor edilen hastaların yönetiminde 6 aylık aralarla 2 tekrar smear alınmasının, HPV testi yapılmasının ve tek seferlik kolposkopi yapılmasının hepsinin güvenli ve etkin yöntemler olduğunu ortaya koymuştur. Bu nedenle de 2001 konsensus önerilerinde bu 3 yaklaşımında ASC-US yönetiminde kullanılabilecek yöntemler olduğu belirtilmiştir.
“Reflex Test” orijinal sıvı bazlı sitolojide veya ayrıca alınan bir örnekte HPV çalışılmasına verilen bir isimdir. Bu yaklaşım anormal sitolojisi çıkan kadınların tekrar HPV testi için geri gelmesine gerek bırakmaz ve gereksiz kolposkopiyi önler.
Tek bir kolposkopi incelemesi önemli oranda servikal lezyonu atlayabileceği için ilave takip gerekebilmektedir. ALTS çalışması farklı postkolposkopi takip şemaları önermektedir ve başlangıç kolposkopiden sonraki 12.ayda uygulanan HPV testinin 6 ay aralarla uygulanan iki tekrar smear’a eşdeğer olduğunu tespit etmiştir. Sitoloji ile HPV testini kombine etmek sensitiviteyi arttırmamış ve spesifiteyi düşürmüştür.
Özel Hasta Popülasyonları , ASCUS Belirtileri nelerdir , ASCUS hakkındaki tüm sorular
ASC-US tespit edilen kadınlardaki HPV-DNA pozitifliği kadın yaşıyla değişkenlik gösterir. Genç kadınlardaki HPV DNA pozitifliği daha yaşlı olanlara göre daha fazladır. Bu nedenle adelosan popülasyonda HPV DNA testini kullanmak daha fazla oranda hastanın kanser açısından düşük riskli olmasına rağmen kolposkopiye yönlendirilmesine neden olur. ASC-US postmenopozal kadınlarda premenopozal kadınlarfa göre daha az görülür ve bu yaş grubunda önemli bir patoloji bulma oranı daha düşüktür. HPV testi ASC-US tespit edilen daha yaşlı kadınlarda gençlere göre daha etkindir çünkü daha az oranda kadının kolposkopiye gitmesine neden olur.
ASC-US, HIV infeksiyonu olan kadınlarda sık görülen bir durumdur. Daha önceki çalışmalarda bu hasta popülâsyonunda HPV-DNA pozitifliğinin yüksek oranda olduğu rapor edilmiştir. Bu nedenle de tüm immünsüprese kadınların kolposkopiye gitmesi önerilmiştir. Daha yeni çalışmalar öncekilere kıyasla daha düşü oranda HPV pozitifliği ve CIN 2,3 rapor etmiştir ve bu nedenle de immünsupresyonu olan kadınların genel popülâsyondaki kadınlar gibi yönetilmesini önermiştir. Gebe kadınlarda ASC-US tespit edildiğinde kanser riski oldukça düşüktür bu nedenle de antepartum kolposkopik değerlendirme yönetime eklenmemiştir.
ASC-US Tespit Edilen Kadınların Yönetimi
Genel Yaklaşım
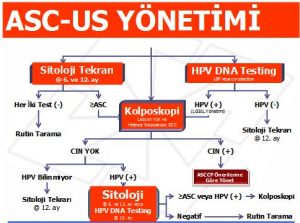
Belli aralarla tekrar sitoloji, HPV DNA testi veya direkt kolposkopi ASC-US tespit edilen 20 yaşın üzerindeki kadınların yönetiminde kabul edilebilir yöntemlerdir. Sıvı bazlı sitoloji kullanıldığında “refleks HPV” testi tercih edilen bir yöntem olabilir.
HPV-DNA negatif ASC-US‘lu kadınlar 12. ayda tekrar sitoloji ile değerlendirilebilir. HPV-DNA pozitif kadınlar ise LSIL ile aynı şekilde yönetilir ve kolposkopiye yönlendirilir. Görülen bir lezyonu olmayan veya kolposkopi yetersizse kadınlarda endoservikal örnekleme tercih edilir. Kolposkopisi yeterli ve transformasyon zonunda lezyonu tespit edilen kadınlarda ise endoservikal örnekleme kabul edilebilir bir yaklaşımdır. Kolposkopi sonrası HPV pozitif fakat CIN negatif kadınlar 12. ayda HPV DNA testi veya 6 ve 12. aylarda tekrar sitoloji ile değerlendirilebilir. HPV DNA testinin 12. aydan kısa aralarla uygulanmaması önerilmektedir.
Eğer ASC-US yönetiminde tekrar sitoloji kullanılacaksa sitoloji tekrarlarının 6 ay aralarla en az 2 ardışık test negatif çıkıncaya kadar devam etmesi önerilir. Tekrar sitolojilerde ASC-US veya üzerinde bir lezyon tespit edilirse kolposkopi önerilir.Eğer 2 sitoloji negatif gelirse hasta normal takip programına alınır.
Eğer ASC-US yönetiminde kolposkopi kullanılacaksa CIN tespit edilmeyen hastada 12. ayda tekrar sitoloji önerilir. CIN tespit edilen hasta uygun ASCCP önerilerine göre takip edilir.
ASC-US’un başlangıç yönetiminde rutin tanısal eksizyonel girişim kabul edilen bir yaklaşım değildir (Şekil 3).
Özel Popülasyonlarda ASC-US Yönetimi (Tedavisi )
Adelosan Kadınlar
Adelosanlar ASC-US tespit edilen kadınlarda 12. ayda sitoloji tekrarı önerilmektedir.12. ayda sadece HSIL veya üzerinde lezyon tespit edilenler kolposkopiye yönlendirilir. 24 aylık takipden sonra ASC-US veya üzerinde lezyon tespit edilen kadınlar kolposkopiye yönlendirilir (Şekil 4).
İmmünsüprese Kadınlar
HIV ile enfekte veya diğer nedenlerle immünsuprese olan kadınlar genel popülasyondaki kadınlar ile aynı şekilde yönetilir.
Gebe Kadınlar
20 yaşın üzerinde gebe ve ASC-US tespit edilen kadınlar gebe olmayan kadınlarla aynı şekilde yönetilir sadece tek istisna kolposkopinin postpartum 6. haftaya ertelenmesidir. Gebe kadınlarda endoservikal küretaj kabul edilen bir yaklaşım değildir.
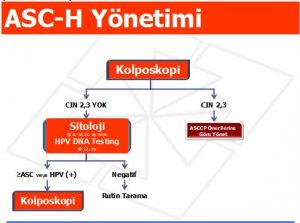
ASC-H Yönetimi (Tedavisi )
ASC-H’in kabul edilen yönetimi hastanın direkt kolposkopiye yönlendirilmesidir. CIN 2,3 saptanmayan hastalarda HPV-DNA testi ile 12. ayda takip veya 6. ve 12. aylarda sitolojik tarama yapılmalıdır. Takipde HPV-DNA testi pozitif olanlar veya asc-us ve üzerinde sitolojik anormallik tespit edilenler kolposkopiye yönlendirilmelidir. Eğer HPV DNA negatifse veya ardı ardına iki sitoloji taramasi negatifse hasta rutin takip programına alınmalıdır (Şekil 5).
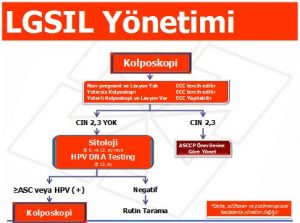
LSIL tedavisi
Geçen dekadda ABD’de tespit edilen LSIL oranı artmıştır ve 2003’de sıvı bazlı sitolojilerde LSIL oranı %2.9’a yükselmiştir. LSIL oranı HPV enfeksiyonunun iyi bir göstergesidir. Yeni yapılan bir metaanalizde LSIL tespit edilen hastalarda yüksek riskli HPV-DNA pozitifliği %76.6 tespit edilmiştir. LSIL’de başlangıç kolposkopide CIN 2 veya daha ciddi bir lezyon saptanma oranı ise %12-16 olarak tespit edilmiştir.
ALTS çalışmasından elde edilen veriler ASC-US ve LSIL tespit edilen yüksek riskli HPV DNA pozitif hastalarda CIN 2,3 tespit edilme oranının aynı olduğunu göstermiştir. Bu da bu iki grup hastanın aynı şekilde yönetilmesini desteklemektedir (postmenopozal hastalar hariç).
LSIL Yönetimi
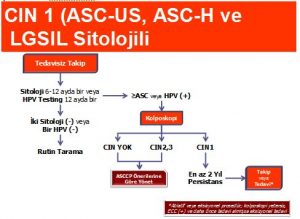
LSIL hastalarının yönetiminde bazı özel hasta grupları hariç kolposkopi önerilmektedir. Endoservikal örnekleme kolpokopide bir lezyon tespit edilemeyen gebe olmayan kadınlarda ve kolposkopi yetersiz olduğunda tercih edilen(preferred) bir yaklaşımdır fakat yeterli kolposkopi yapılan ve transformasyon zonunda lezyon tespit edilen kadınlarda ise kabul edilebilir (acceptable) bir yaklaşımdır. CIN 2,3 tespit edilmeyen LSIL hastalarında kolposkopi sonrası 12. ayda HPV testi veya 6. ve 12.aylarda tekrar sitoloji yapılmalıdır.
Eğer HPV DNA negatif ise veya ardışık 2 sitolojik tarama negatifse hasta rutin tarama programına alınabilir. Eğer HPV DNA pozitifse veya tekrar sitolojilerde ASC-US veya üzerinde bir lezyon rapor edilirse kolposkopi önerilmelidir. CIN tespit edilen kadınlar ASCCP’nin uygun guideline’ına göre yönetilmelidir. LSIL tespit edilen bir hastanın başlangıç yönetiminde, CIN yoksa diagnostik eksizyonel veya ablatif yöntemlerin uygulanması kabul edilebilir bir yaklaşım değildir (Şekil 6).
Özel Popülasyonlarda LSIL Yönetimi
Adelosan
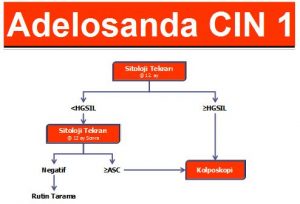
Adelosanlarda LSIL tespit edilirse yıllık sitolojik takip önerilir. 12 aylık takipte sadece HSIL veya daha yüksek derecede bir lezyonu olanlar kolposkopiye yönlendirilir.24 aylık takipte ASC-US veya üzerinde lezyon tespit edilenler kolposkopiye yönlendirilir. Adelosan LSIL tespit edilen hastalarda, HPV DNA testi kabul edilebilir bir yaklaşım değildir. Eğer HPV DNA testi uygulandıysa bile bu hastanın yönetimini değiştirmemelidir.
Postmenopozal Kadınlar
Postmenopozal LSIL’li kadınların yönetiminde “refleks HPV” ,6 ve 12. aylarda tekrar sitoloji ve kolposkopi kabul edilebilir yaklaşımlardır. Eğer HPV DNA testi negatifse veya kolposkopide CIN tespit edilmediyse 12.ayda servikal sitoloji önerilir. Eğer HPV DNA testi pozitif veya tekrar sitolojide ASC-US veya üzerinde lezyon varsa kolposkopi önerilmelidir.Eğer ardışık 2 sitoloji negatifse hasta rutin takip programına alınmalıdır.
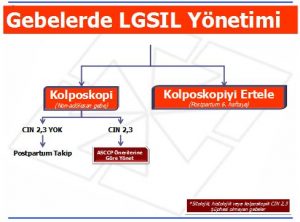
Gebe Kadınlar
Adelosan olmayan gebe kadınlarda kolposkopi tercih edilir. Gebe kadınlarda endoservikal küretaj kabul edilebilir bir yöntem değildir. Başlangıç kolposkopiyi postpartum 6.hafta sonraya ertelemekde kabul edilebilir bir yaklaşımdır. Gebe kadınlarda başlangıç kolposkopide sitolojik,histolojik,kolposkopik olarak CIN 2,3 ‘den şüphelenilmiyorsa postpartum takip önerilebilir. Bu tür kadınlarda ilave kolposkopik veya sitolojik değerlendirme gereksiz ve kabul edilemez bir yaklaşımdır (Şekil 7).
HSIL Nedir HSIL Nasıl Tedavi Edilir
ABD’deki labaratuarlarda HSIL rapor etme oranı %0.7’dir.HSIL oranı yaşla birlikte değişim göstermektedir. Bir merkezde 20-29 yaş arasında HSIL oranı %0.6 iken 40-49 yaş grubunda %0.2 50-59 yaş grubunda %0.1 olarak tespit edilmiştir.Sitolojik olarak HSIL tespit edilmiş olması servikal neoplazi açısından önemli bir risk taşır. HSIL tespit edilen hastalarda tek kolposkopik inceleme ile CIN2 saptanma oranı %53-66 arasında, LEEP ile eksizyonel biopsi yapılan HSIL olgularında ise bu oran %84-97 arasında değişmektedir. HSIL tespit edilen hastaların yaklaşık %2’de invaziv kanser tespit edilir.
HSIL tespit edilen hastalarda belirgin oranda CIN 2 ve HPV DNA tespit etme riski vardır.Bu hastalarda HPV testi veya sitoloji ile triaj uygun değildir. Kolposkopi önemli oranda CIN2,3 lezyonunu kaçırabileceği için bu hastalarda kolposkopinin CIN 2,3 tespit edememesi CIN 2,3 lezyonlarının olmadığı anlamına gelmez.Sonuç olarak HSIL tanısı alan birçok hasta tanısal eksizyonel bir prosedüre maruz kalacaktır.Bu nedenle de birçok yazar HSIL olgularında LEEP ile gör ve tedavi et (see-and-treat) yaklaşımını önermektedir. Bununla birlikte, adelosan ve genç erişkinlerdeki birçok CIN 2,3 olgusunun spontan regrese olacağı da akılda tutulmalıdır.
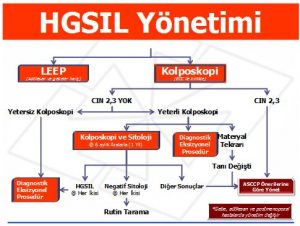
HSIL Olgularının Yönetimindeki Öneriler
HSIL olgularının yönetiminde direkt kolposkopi veya LEEP ile diagnostik tanısal girişim kabul edilebilir yöntemlerdir (sadece bazı özel hasta grupları hariç).Eğer histolojik olarak CIN 2,3 tespit edilemezse bir yıl süreyle 6 aylık aralarla kolposkopik veya sitolojik takip önerilir.Bu durumda kolposkopi yeterli ve endoservikal küretaj negatif olmalıdır.Bu şartlar altında sitolojik,histolojik ve kolposkopik bulguların tekrar gözden geçirilmesi de kabul edilebilir bir yaklaşımdır.Eğer tanı değişir ise yönetim yeni tanıya göre değiştirilir.Eğer sitoloji ve kolposkopi ile izlem seçilirse 6 veya 12. aylarda tekrar sitolojide HSIL tespit edilirse tanısal bir eksizyonel girişim önerilir.Bir yıllık takipten sonra 2 ardışık sitoloji negatifse hasta rutin takip programına alınabilir.
Kolposkopisi yetersiz olan HSIL olgularında tanısal bir eksizyonel girişim önerilir ( gebeler hariç). CIN 2,3 tespit edilen hastalar ASCCP’nin buna uygun önerilerine göre yönetilir. Ablatif yöntemler aşağıdaki durumlarda kabul edilemez;
Kolposkopi uygulanmadıysa
Histolojik olarak CIN 2,3 tanısı yoksa,
Endoservikal örneklemede herhangi derecede bir CIN tespit edilmişse.
HPV DNA veya sitoloji ile triaj kabul edilebilir yaklaşımlar değildir (Şekil 8)
Özel Popülasyonlarda HSIL Yönetimi
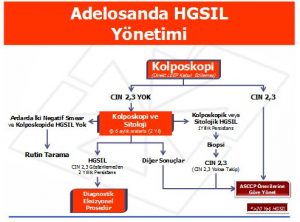
Adelosan Kadınlar
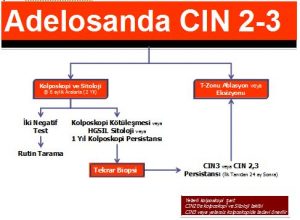
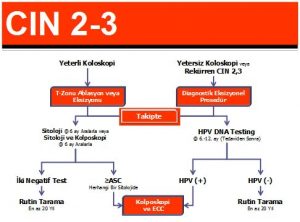
Adelosanlarda HSIL tespit edildiği zaman kolposkopi önerilmektedir.LEEP ile gör ve tedavi et yaklaşımı adelosan kadınlarda kabul edilebilir bir yaklaşım değildir. Histolojik olarak CIN2,3 tespit edilemezse 24 aya kadar 6 aylık aralarla kolposkopi veya sitoloji ile takip tercih edilir ki bu durumda kolposkopi yeterli ve endoservikal değerlendirme negatif olmalıdır. Bazı istisnasi durumlarda eksizyonel tanısal girişimler kabul edilebilir.Eğer HSIL takibinde,kolposkopik olarak HSIL tespit edilirse veya sitolojide HSIL bir yıl boyunca persiste ederse biopsi önerilebilir.Histolojik olarak CIN 2,3 tespit edilirse uygun ASCCP önerilerine göre hasta yönlendirilir.Eğer HSIL 24 ay boyunca histolojik olarak CIN 2,3 tespit edilmeden persiste ederse tanısal bir ekzisyonel girişim önerilir.Ardışık 2 negatif sitoloji sonrası HSIL’li adelosan ve genç kadınlar normal takip programına alınabilir.Eğer adelosanda HSIL tespit edildikten sonra yapılan kolposkopi yetersizse veya endoservikal değerlendirmede herhangi bir derecede CIN tespit edilirse tanısal bir eksizyonel girişim önerilir (Şekil 9).
Gebe Kadınlar
Gebe kadınlarda HSIL tespit edilirse kolposkopi önerilir.Kolposkopinin gebeliğin oluşturduğu kolposkopik değişiklikleri iyi bilen ve değerlendirebilen bir kolposkopist tarafından yapılması önerilir.CIN 2,3 veya kanser şüphesi uyandıran lezyonların biopsi yapılması tercih edilir diğer lezyonlar içinde biopsi yapılması kabul edilebilir.Gebe kadınlarda endoservikal küretaj kabul edilen bir yöntem değildir.Sitoloji kolposkopi veya servikal biopside invasiv kanser şüphesi olmadıkça tanısal eksizyonel girişim kabul edilebilir bir yaklaşım değildir. HSIL tanısı alan fakat CIN2,3 tespit edilmeyen gebe kadınlarda sitoloji ve kolposkopi ile postpartum 6 haftadan önce değerlendirme önerilmez.
Atipik Glandüler Hücreler (AGC) Nedir ? AGC nasıl Tedavi Edilir ?
AGC nadir olarak tespit edilir.2003’de ABD’de sadece %0.4 oranında rapor edilmiştir. AGC’ler reaktif değişiklikler,polip vb. benign durumlar tarafından sık olarak oluşturulmasına rağmen klinisyenlerin AGC rapor edilen hastalarda altta yatan anormal bir servikal,endometriyal veya ovaryen bir adenokarsinoma olup olmadığı konusunda dikkatli olması gereklidir. Son araştırmalar AGC rapor edilen olguların %9-38’de önemli bir neoplazi (CIN 2,3,AIS veya kanser) olduğunu %3-17’de invasiv kanser olduğunu bildirmektedir.
AGC rapor edilen hastalarda altda yatan anormalikler yaşla birlikte değişkenlik gösterir. Değişik oranlarda glandüler anormalikler tespit edilmekle birlikte CIN en sık tespit edilen anormalliktir. Jinekolojik malignansi riski 35 yaşın altındaki kadınlarda üstündekilere oranla daha düşüktür. Gebelik AGH ile jinekolojik malignite arasındaki ilişkiyi değiştirmemektedir.
HPV testş veya tekrar sitoloji AGC rapor edilen hastaların ilk yönetiminde kullanılması durumunda altda yatan anormallikleri güvenilir sensitivitede yakalamak için yeterli değildir. AGH’lerle ilişkili neoplazilerin geniş spektrumu dolayısıyla başlangıç değerlendirme birçok testi içermelidir. Bunlar kolposkopi, endoservikal küretaj ve örnekleme, HPV testi ve endometrial değerlendirmedir. Bu hastalardaki yüksek malignite riski ve başlangıç değerlendirme testlerinin kötü sensitivitesi nedeniyle tanısal eksizyonel girişim gerekebilir.
Diğer Glandüler Anormallikler
40 yaşın üzerindeki kadınlarda sitolojide benign görünümlü endometrial hücreler,endometrial stromal hücreler veya histiositler nadiren görülür. 40 yaın üzerindeki kadınlardan alınan servikal sitoloji spesmenlerinin %0.5-1.8’de endometrial hücreler tespit edilir. Premenopozal hastalarda benign görünümlü endometriyal hücreler nadiren önemli bir patoloji ile ilişkilidir. Benzer şekilde endometriyal stromal hücrelerin veya histiositlerinde bu grupta nadiren bir klinik önemi vardır.Bunun aksine,postmenopozal kadınlarda benign görünümlü endometriyal hücreler nadir olmayarak önemli endometriyal patolojilerle birlikte olabilir. Hormon replasman tedavisi endometriyal hücrelerin dökülmesini arttırmasına rağmen bu durumda da altda yatan önemli bir endometriyal patoloji ihtimali vardır. Benign görünümlü endometriyal hücreler küçük aksesuar kanallar,benign adenozis veya histerektomi sonrası fallop tüpünün vajene prolabe olması nedeniyle saptanabilir ve bunların klinik bir önemi yoktur.
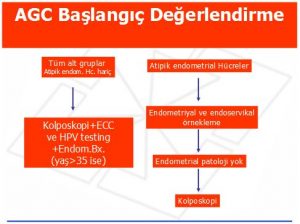
AGC Saptanan Kadınların Yönetimi
Başlangıç Değerlendirme
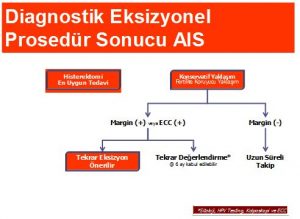
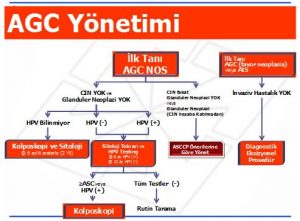
AGC ve AIS tespit edilen tüm kadınlarda başlangıç değerlendirmede endoservikal örnekleme önerilir. Endometriyal örnekleme ise 35 yaşın üzerindeki kadınlarda kolposkopi ve endoservikal örneklemeye ek olarak AGC ve AIS rapor edilen tüm hastalara önerilir. Endometriyal örnekleme ayrıca 35 yaşın altında olan fakat endometrial bir neoplaziyi düşündüren klinik bulgusu (anormal vajinal kanama, kronik anovülasyon vb ) tüm kadınlara da önerilir. Atipik endometriyal hücreler tespit edilen kadınların başlangıç değerlendirilmesinde de endoservikal ve endometriyal örnekleme önerilir. Kolposkopi başlangıçta uygulanabileceği gibi biopsi sonuçları öğrenildikten sonra da yapılabilir. Eğer endometriyal bir patoloji saptanmadı ise kolposkopi önerilir. Eğer daha önceden yapılmadı ise atipik enservikal, endometrial veya başka şekilde tanımlanamayan atipik glandüler hücreler rapor edilen hastada kolposkopi sırasında HPV DNA testi yapılması tercih edilir.Tek başına HPV DNA testi veya tekrar sitoloji AGC veya AIS tanısı olan hastaların yönetiminde uygun değildir (Şekil 10).
AGC Takibi
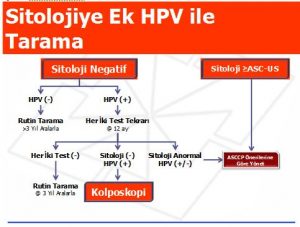
HPV durumu bilinen ve smear sonucu AGC, atipik endometriyal hücreler, glandüler neoplazi-NOS rapor edilen ve CIN veya diğer neoplazi tespit edilmemiş hastada kolposkopi sonrası izlemde eğer HPV DNA pozitifse 6.ayda HPV DNA tekrar test edilir, eğer HPV DNA negatifse 6.ayda HPV DNA testi yapılır. Eğer takipte onkojenik HPV DNA pozitif çıkarsa veya ASC-US ve üzerinde sitolojik anormallik varsa hasta kolposkopiye yönlendirilir. Eğer her iki testte negatifse hasta rutin takibe alınır. HPV durumu bilinmeyen ve smear sonucu AGC, atipik endometriyal hücreler, glandüler neoplazi-NOS rapor edilen ve CIN veya diğer neoplazi tespit edilmemiş hastada kolposkopi sonrası izlemde 6 ay arayla sitoloji tekrarı yapılır. Ardışık 4 negatif test sonrasında hasta rutin takip programına alınır.
Eğer başlangıç değerlendirmede CIN tespit edilmiş fakat glandüler neoplazi tespit edilmemişse hasta ASCCP’nin uygun önerilerine göre yönlendirilir. AGC-favor neoplasia veya endoservikal AIS saptanan bir hastada eğer başlangıç değerlendirmede invaziv hastalık saptanmadı ise tanısal bir eksizyonel girişim önerilir. Uygulanacak tanısal eksizyonel girişimin cerrahi sınırları intakt ve yorumlanabilir bir şekilde sağlaması önemlidir. Aynı anda endoservikal örneklemede tercih edilir (Şekil 11).
Histolojik Anormalliklerin ASCCP’ye göre Yönetimi
Histolojik olarak tanısı CIN1,2,3 veya AIS çıkan hastaların yönetimi ise şekil 13 -17 de özetlenmiştir.
Sonuç
Klinikde sık olarak karşılaştığımız patolojilerin yönetimi için oluşturulan “guideline” ve “algoritmalar” kanıta dayalı olarak geliştirilmelerine rağmen bir çok klinik durumla ilgili iyi kalite veri bulunmamaktadır. Bu gibi durumlarda da konuyla ilgili kişilerin görüşü “uzman görüşü” önem kazanmaktadır. Fakat şunu hiçbir zaman unutmamak gerekir ki “guideline” lar asla doktorun “klinik değerlendirmesi” nin önüne geçmemelidir çünkü klinikte karşılaştığımız her durum için uygun bir “algoritma ve guideline” her zaman yoktur.
Kolposkopi Nedir Nasıl Yapılır
HPV 16 HPV 18 ASCUS Tanı ve tedavisi
HPV 16 HPV 18 ve diğer yüksek riskli HPV pozitif çıkan kadınlar, ASCUS (önemi belirlenemeyen atipik hücreler ), LSIL, HSIL , ASC-H , AGC smear sonucu olan hastalar bu konuda deneyimli jinekologlar tarafından değerlendirilmelidir. Bu tür lezyonların değerlendirilmesinde HPV testi ve kolposkopi çok önemlidir. Kolposkopi bu konuda deneyimli jinekologlar tarafından yapılmalıdır. Prof Dr Polat Dursun ülkemizdeki HPV sıklığı ve HPV tipleri, Türkiye’deki sitoloji anormalliklerin sıklığı , Türkiyedeki ASCUS, LSIL, HSIL sıklığı hakkında ilk çalışmaları yapıp uluslararası literatürde yayınlamıştır. Bu çalışmaların özetleri aşağıda bulunabilir. Ankara’da HPV tanısı ve HPV’nin yol açtığı ASCUS, LSIL, HSIL, ASC-H, AGC gibi lezyonların tanı ve tedavisi ve Kolposkopik değerlendirilmesi Prof Dr Polat Dursun tarafından yıllardır başarı ile yapılmaktadır.
https://www.ncbi.nlm.nih.gov/pubmed/24022311
HPV types in Turkey: multicenter hospital based evaluation of 6388 patients in Turkish gynecologic oncology group centers.
https://www.ncbi.nlm.nih.gov/pubmed/19948015
Human papillomavirus (HPV) prevalence and types among Turkish women at a gynecology outpatient unit.
https://www.ncbi.nlm.nih.gov/pubmed/19541303
Prevalence of cervical cytological abnormalities in Turkey.
https://www.ncbi.nlm.nih.gov/pubmed/19432612
Women’s knowledge about human papillomavirus and their acceptance of HPV vaccine.
Kaynaklar
1. 1.Hacer Uyanıkoğlu Uzmanlık Tezi. Servikal Kanser Taramasında Asetikasit Sonrası İnspeksiyonla (Vıa), Servikal Smear’in Karşılaştırılması.
2. 2.Jemal A, Murray T, Samuels A, Ghafoor A, Ward E, Thun MJ. Cancer statistics, 2003. CA Cancer J Clin 2003;53:5-26.
3. 3.Cronje HS. Screening for cervical cancer in developing countries. Int J Gynecol Obstet 2004;84:101-8.
4. 4.Novak’s gynecology, 13th edition: By Jonathan S. Berek. Philadelphia: Lippincott Williams & Wilkins Publishers, 2002.
5. 5.van Oortmarssen GJ, Habbema JD. Epidemiological evidence for age-dependent regression of pre-invasive cervical cancer. Br J Cancer 1991;64:559-65.
6. 6.Bovicelli A, Bristow RE, Montz FJ. HPV testing: where are we now? Anticancer Res 2000;20:4673-80.
7. 7.Helmerhorst TJ, Meijer CJ. Cervical cancer should be considered as a rare complication of oncogenic HPV infection rather than a STD. Int J Gynecol Cancer 2002;12:235-6.
8. 8.Walboomers JM, Jacobs MV, Manos MM, Bosch FX, Kummer JA, Shah KV, Snijders PJ, Peto J, Meijer CJ, Munoz N. Human papillomavirus is a necessary cause of invasive cervical cancer worldwide. J Pathol 1999;189:12-9.
9. 9.Woodman CB, Collins S, Winter H, Bailey A, Ellis J, Prior P, Yates M, Rollason TP, Young LS. Natural history of cervical human papillomavirus infection in young women: a longitudinal cohort study. Lancet 2001;357:1831-6.
10. 10.ACOG Practice Bulletin: clinical management guidelines for obstetrician-gynecologists. Number 45, August 2003. Cervical cytology screening. Obstet Gynecol 2003;102:417-27.
11. 11.Fey MC, Beal MW. CEU: Role of human papilloma virus testing in cervical cancer prevention. J Midwifery Womens Health 2004;49:4-13.
12. 12.Meijer CJ, Snijders PJ, van den Brule AJ. Screening for cervical cancer: should we test for infection with high-risk HPV? CMAJ 2000;163:535-8.
13. 13.Steller MA. Cervical cancer vaccines: progress and prospects. J Soc Gynecol Investig 2002;9:254-64.
14. 14.Austin RM. College of American Pathologists Conference XXX on quality and liability issues with the Papanicolaou smear: introduction. Arch Pathol Lab Med 1997;121:227-8.
15. 15.American Cancer Society. Cancer facts and figures for Hispanics 2000-2001. Atlanta, GA: American Cancer Society, 2001.
16. 16.Quinn M, Babb P, Jones J, Allen E. Effect of screening on incidence of and mortality from cancer of cervix in England: evaluation based on routinely collected statistics. BMJ 1999;318:904-8.
17. 17.Spitzer M. In vitro conventional cytology historical strengths and current limitations. Obstet Gynecol Clin North Am 2002;29:673-83.
18. 18.Cervical cancer. NIH Consens Statement 1996;14:1-38;quiz 4p.
19. 19.Hutchinson ML, Berger BM, Farber FL.Clinical and cost implications of new technologies for cervical cancer screening: the impact of test sensitivity. Am J Manag Care 2000;6:766-80.
20. 20.Sawaya GF, Grimes DA. New technologies in cervical cytology screening: a word of caution. Obstet Gynecol 1999;94:307-10.
21. 21.Wright TC Jr, Massad LS, Dunton CJ, Spitzer M, 21. Wilkinson EJ, 21. Solomon D; 2006 American Society for Colposcopy and Cervical Pathology-sponsored Consensus Conference.2006 consensus guidelines for the management of women with abnormal cervical cancer screening tests. Am J Obstet Gynecol. 2007 Oct;197(4):346-55. Review
Not :Tüm algoritimler www.asccp.org adresinden temin edilmiş ve Türkçeleştirilmiştir.
Tablo 1 : ABD’de Servikal Kanser Taramasındaki Başarısızlıkların Nedenleri
Neden Sayı ( % )
Taramanın uygulanmamış olması 6,280 ( %50 )
Kötü tarama 1,260 ( %10 )
Hasta izleminde hatalar 1,260 ( %10 )
Örnekleme ve yorumlamada hatalar 3,770 ( %30 )
Toplam 12,560 ( %100 )
Tablo 2 : Farklı tarama sıklıklarında kümülatif servikal kanser azalma oranları
Tarama Sıklığı Kanserde azalma oranı
1 yıl %93
2 yıl %93
3 yıl %91
5 yıl %84
10 yıl %64
IARC,1986’dan uyarlanmıştır.
ŞEKİLLER